Модификация природных аминокислот — процесс происходящий в нашем организме под действием специальных ферментов. Одним из самых распространенных путей модификации является окисление одного из атомов углерода в молекуле аминокислоты. При этом связь углерод-водород превращается в связь углерод-гидроксогруппа (-OH). К примеру, такой процесс лежит в основе биосинтеза ванкомицина — известного антибиотика.
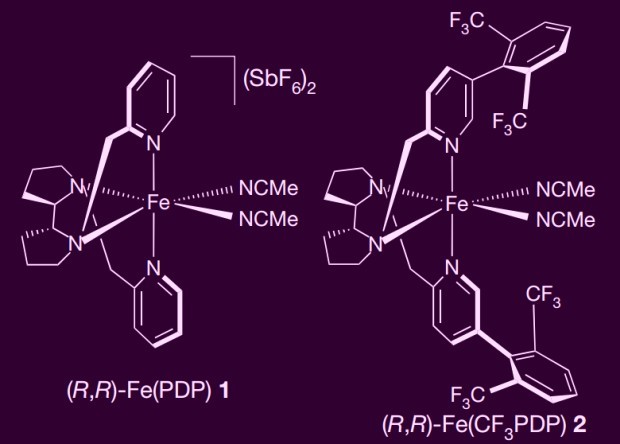
Биосинтез ванкомицина (a). На врезе — структура катализаторов для селективного окисления пролина, валина и лейцина
Thomas J. Osberger et al. / Nature, 2016
Направленное окисление аминокислот идет в нашем организме с помощью специальных катализаторов — белков-ферментов, которые, как правило, содержат в себе атом железа. Однако каждый фермент обладает узкой специализацией — он действует только на одну аминокислоту, или, более того, на одну аминокислоту в определенном белке.
Окисление аминокислот — эффективный путь для создания новых искусственных молекул, используемых, например, в синтезе лекарственных препаратов. Для того, чтобы получить несколько исходных окисленных аминокислот для последующих химических превращений, потребуется соответствующее количество ферментов. Новая работа позволяет сократить этот набор до одного-двух катализаторов.

Схема возможных превращений пролина после окисления перекисью водорода в присутствие железосодержащего катализатора
Thomas J. Osberger et al. / Nature, 2016
Химики предложили заменить сложные белковые катализаторы на низкомолекулярные (небольшие) комплексы железа. Первые эксперименты позволили получить 21 искусственную аминокислоту на основе трех природных и одной искусственной — пролина, валина, норвалина и лейцина. Кроме того, авторы проверили специфичность катализатора на ди- и трипептидах (молекулах, состоящих из двух и трех аминокислотных фрагментов соответственно) — воздействию всегда подвергался строго один и тот же атом углерода в структуре молекулы.

Схема превращения трипептида на основе природных аминокислот в восемь трипептидов, содержащих остатки искусственных аминокислот
Thomas J. Osberger et al. / Nature, 2016
В частности, химикам удалось с помощью каталитического окисления превратить один трипептид в восемь разных трипептидов, содержащих искусственные аминокислоты. По словам авторов, классические подходы потребовали бы восемь различных синтезов «с нуля».
Читать далее
Комментарии:
Авторизуйтесь, чтобы оставить отзыв